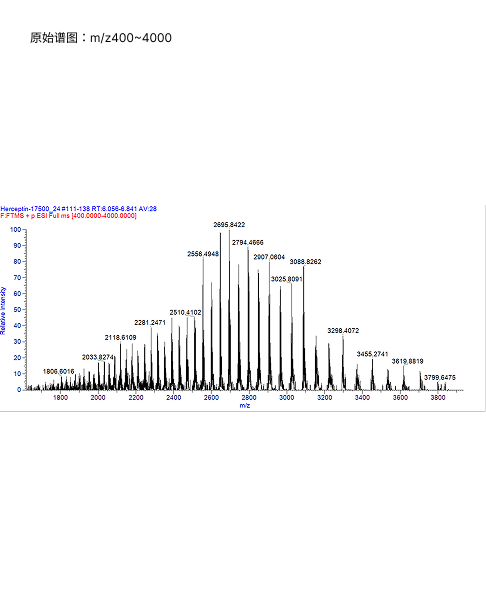
平台介绍
抗体质量研究与分析检测服务,我们深度洞察您在新药研发与注册中面临的结构表征挑战、生物活性验证难题及工艺变更带来的质量可比性风险,严格遵循NMPA/FDA/ICH等国内外法规指南,提供从高级结构与功能表征、纯度/杂质/效价分析,到免疫原性与稳定性评估的全套科学、合规方案,为您的BLA申报奠定坚实基础。
服务阶段:早期发现与筛选、CMC工艺开发、IND申报、临床各期工艺优化与放行、BLA/NDA申报、稳定性研究、上市后变更与持续质量监测。
服务形式:单项检测、方法开发与验证、全流程质量研究、CTD资料撰写、中美欧三地申报技术咨询。
-
-
1000+检测报告
-
150+客户数
-


服务内容
-
0101
一级与高级结构分析
-
覆盖高分辨分子量、序列覆盖率、二硫键配对、翻译后修饰、N/C末端序列分析(Edman和质谱法)、DSC、CD、DLS、SEC-MALS等 核磁和红外等维度结构表征
-
-
0202
电荷异质性与纯度测定
-
等电点(icIEF)、IEX-HPLC
-
糖谱分析
-
基于CE-SDS、SEC/RP的色谱纯度分析
-
-
0303
复杂杂质精细分析
-
深度覆盖产品与工艺相关杂质,国内率先提供质谱法检测 HCP
-
各类微量残留分析
-
-
0404
生物活性与稳定性评价
-
亲和力分析:可提供满足注册要求的抗体FcγRs、FcRn C1q等亲和力分析服务
-
稳定性考察:可提供抗体在长期(-80℃~2-8℃)、加速(2-8℃~25℃)、影响因素评估(3~5个因素)以及冷链运输稳定性考察服务
-
服务优势

-
8年经验
-
1000份报告
-
配备Q-TOF QE/MS、Orbitrap、2D LC、iCIEF/Maurice、AUC、SEC MALS、CD、DSC等先进设备,多种技术联用,满足抗体药物从一级结构到高级结构的全方位分析需求。

尖端仪器平台
-
精通分子量测定、肽图与序列覆盖率分析、翻译后修饰、二硫键配对、糖基化精细分析、聚集体/片段检测、电荷变异体解析、结合活性与生物学活性表征,实现复杂抗体多维度高精度解析。

深度表征能力
-
持续跟踪NMPA、FDA、EMA指导原则,严格遵循2025年版《中国药典》及指导原则、ICH Q6B及Q5C等法规,方案科学合规,降低发补风险与时间成本。

深刻理解监管
-
涵盖方案设计、方法开发与验证、质量表征执行、数据解析及CTD资料撰写,覆盖早期发现、IND、临床各期、BLA/NDA及上市后变更全周期,支持中美欧三地申报,专家全程指导。

全链条一站式
-
8年经验
-
1000份报告
-
尖端仪器平台
配备Q TOF MS/MS、Orbitrap、2D LC、iCIEF/Maurice、AUC、SEC MALS、CD、DSC等先进设备,多种技术联用,满足抗体药物从一级结构到高级结构的全方位分析需求。
-
深度表征能力
精通分子量测定、肽图与序列覆盖率分析、翻译后修饰、二硫键配对、糖基化精细分析、聚集体/片段检测、电荷变异体解析、结合活性与生物学活性表征,实现复杂抗体多维度高精度解析。
-
深刻理解监管
持续跟踪NMPA、FDA、EMA指导原则,严格遵循2025年版《中国药典》及指导原则、ICH Q6B及Q5C等法规,方案科学合规,降低发补风险与时间成本。
-
全链条一站式
涵盖方案设计、方法开发与验证、质量表征执行、数据解析及CTD资料撰写,覆盖早期发现、IND、临床各期、BLA/NDA及上市后变更全周期,支持中美欧三地申报,专家全程指导。
研究依据
-

2025年版《中华人民共和国药典》人用重组单克隆抗体及单抗生物类似药检测章节
-

《抗体偶联药物药学研究与评价技术指导原则》
-

《人用单克隆抗体质量控制技术指导原则》
-

《抗体类产品申报上市药学方面常见问题和审评考虑》
-

《生物制品稳定性研究技术指导原则(试行)》
-

ICH Q6B《质量标准:生物技术产品及生物制品的检测方法及可接受标准》、Q8、Q9、Q10、Q11
-

ICH Q1系列稳定性试验指南(2025年新版合并征求意见稿)
-

ICH Q5C《生物技术/生物制品稳定性试验》
-

ICH Q5E《生物技术/生物制品生产工艺变更可比性研究》
案例展示
关键设备
-
 NMR
NMR -

 Q-EXACTIVE高分辨质谱
Q-EXACTIVE高分辨质谱 -

 Waters Xevo G3
Waters Xevo G3
相关服务
-

ADC 质量研究与检测服务
-


生物大分子质量研究与分析检测服务
即刻联系我们,开启一段"零风险、高价值"的合作之旅
-
质量承诺:
确保您的数据,一次就满足全球最高标准
-
合规承诺:
“零483”的审计记录,“无忧申报”支持
-
速度承诺:
“48小时”标准交付,“24小时”紧急响应
-
价值承诺:
“报告不是终点,而是起点”增值服务