

平台介绍
包材相容性及包装系统密封性研究与分析检测服务,我们聚焦于药品(尤其是注射剂、吸入制剂、滴眼剂等高风险剂型)在研发与申报中面临的包材可提取物/可浸出物(E&L)精准鉴定、生产组件相容性风险及包装系统密封性验证等核心难点,严格遵循NMPA相关技术指南、2025年版《中国药典》药包材标准体系、ICH Q3E及USP <1207>等国内外法规要求,提供涵盖包材适用性评价、可提取物与可浸出物全谱分析、生产组件(硅胶管/滤芯/一次性系统)相容性研究、包装系统密封性验证(真空衰减/高压放电/氦质谱/微生物挑战等确定性方法)及毒理学风险评估的全套合规方案,助力您的项目顺利通过技术审评。

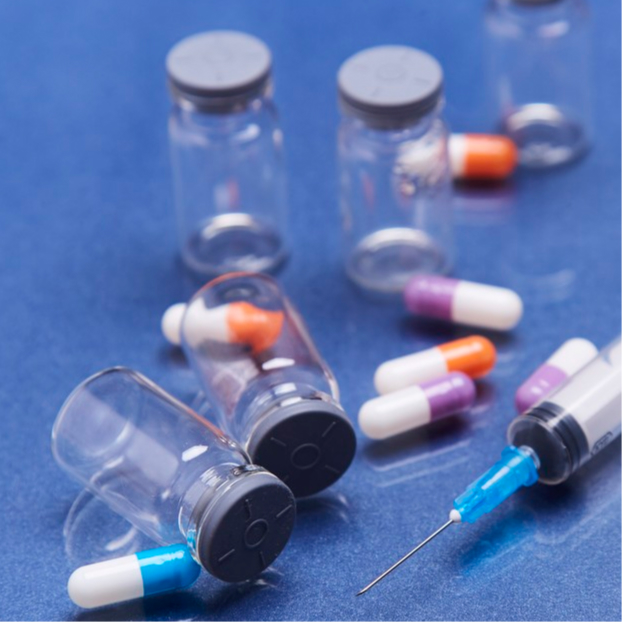

-
相容性研究
-
提取研究
采用高温、长时间或强溶剂等强化条件,结合模拟溶剂,全面筛查包装材料中的可提取物,建立提取物谱。
-
迁移与吸附研究
在实际储存条件下检测浸出物水平,同时评估药品有效成分或辅料是否被包装材料吸附导致含量下降。
-
安全性评估
参照SCT(安全性关注阈值)与QT(界定阈值),对浸出物进行毒理学风险评估;超过QT者通过PDE(每日允许暴露量)计算严格控制。

-
-
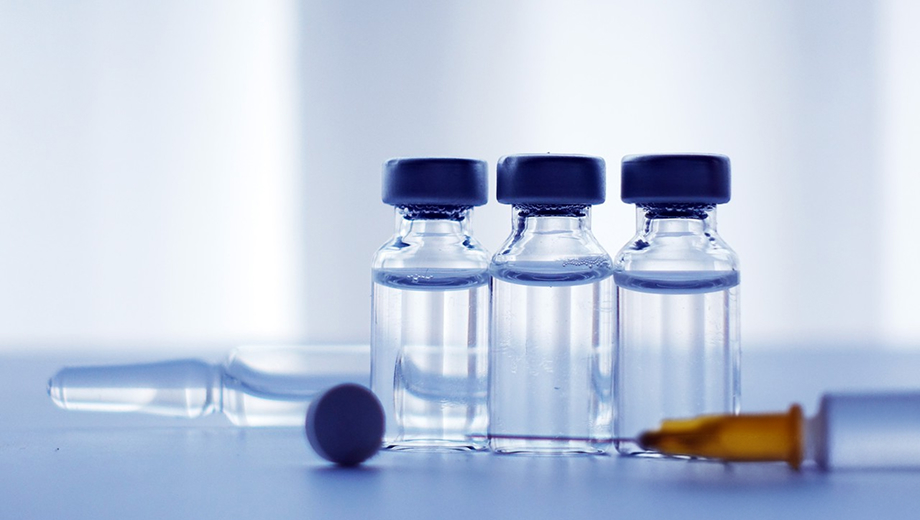
包装密封性CCIT
-
真空衰减法
首选方法,适用于西林瓶、安瓿瓶、预灌封注射器、输液袋等,可检≥1μm微泄漏,无损、定量、灵敏度高。
-
高压放电法
适用于高粘度、混悬液、生物制剂,可解决真空法对粘稠液的检测盲区。
-
微生物挑战法
包装密封性验证的“金标准”,直接验证防微生物侵入能力。
-
示踪气体法(氦质谱法)
适用于研发验证阶段及高风险无菌制剂,可检出≤0.1μm微小漏孔。
-
服务优势

-
GMP
-
FDA 21
CFR Part 11
-
实验室硬件
GC-QTOF/GC-MS/HS-GC-MS/GC-MSMS/LC-QTOF/UPLC-MSMS/ICP-MS等国际一流设备
-
服务制剂
注射剂、滴眼剂、吸入制剂、口服液体制剂、注射剂、滴眼剂、吸入气雾剂
-
服务对象
包括西林瓶、安瓿瓶、预灌封注射器、卡式瓶、塑料瓶、输液袋、胶塞、铝盖等各类包装组件,以及过滤器、硅胶管等一次性使用系统组件
研究依据
-

2025年版《中国药典》9621《药包材通用要求指导原则》及9628《无菌药品包装系统密封性指导原则》
-

2025年版《中国药典》“1+4+58”药包材标准体系(1项通用指导原则+4项材质指导原则+58项通用检测方法)
-

《化学药品注射剂包装系统密封性研究技术指南(试行)》(CDE 2020年第33号通告)
-

《化学药品注射剂生产所用的塑料组件系统相容性研究技术指南(试行)》(CDE 2020年第33号通告)
-

FDA 21 CFR Part 11(数据完整性要求)
-

USP <1207>(容器密封完整性测试)、USP <1663>/<1664>(提取物与浸出物评估)
-

ICH Q3D、ICH Q3E
-

《化学药品注射剂与塑料包装材料相容性研究技术指导原则(试行)》
-

EP 3.2.2(塑料容器用于药物制剂)
研究流程
关键设备
-
 电感耦合等离子体质谱仪
电感耦合等离子体质谱仪 -

 高分辨质谱仪
高分辨质谱仪 -

 高效液相色谱仪
高效液相色谱仪 -

 气相色谱仪
气相色谱仪 -

 液相色谱质谱联用仪
液相色谱质谱联用仪
相关服务
即刻联系我们,开启一段"零风险、高价值"的合作之旅
-
质量承诺:
确保您的数据,一次就满足全球最高标准
-
合规承诺:
“零483”的审计记录,“无忧申报”支持
-
速度承诺:
“48小时”标准交付,“24小时”紧急响应
-
价值承诺:
“报告不是终点,而是起点”增值服务







